Baggrundsartikel
9.1 Indikation for parathyreoidectomi
Ved en international konsensus- konference i år 2009 er der udarbejdet guidelines for henvisning af patienter med asymptomatisk PHPT til PTX (71-73). I guidelines understreges det, at PTX altid bør overvejes hos patienter med PHPT, da indgrebet forventelig fører til, at sygdommen kureres hos mere end 90 % (oftest >95 %) af patienterne (74;75). I særdeleshed er der grund til at henvise patienter til PTX, hvis de opfylder et eller flere af de kriterier, som er anført i faktaboks 7.
Det bemærkes, at manglende visualisering af evt. forstørrede glandler ved præoperativ lokalisationsdiagnostik ikke taler imod at der forsøges kurativ kirurgisk behandling (72).
Faktaboks 7. Indikation for parathyreoidektomi (PTX)

9.2 Præoperativ medicinsk behandling
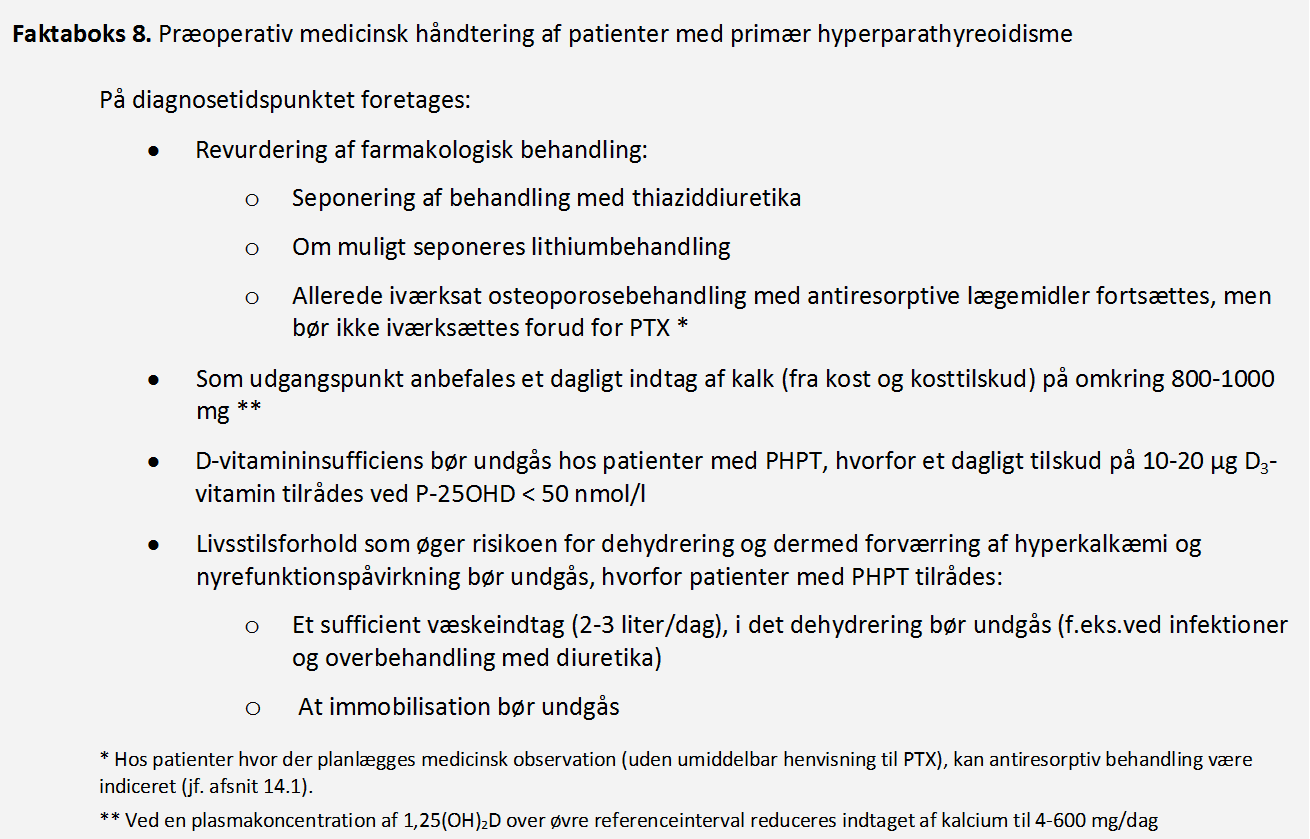
For patienter som henvises til PTX tilrådes forholdsregler som anført i faktaboks 8 i perioden fra diagnosen er stillet og frem til operationstidspunktet.
Medicinsk behandling af patienter som ikke umiddelbart henvises til operation er beskrevet i afsnit 14.
9.2.1 Antiresorptiv behandling forud for parathyreoidektomi
Behandling med lægemidler som mindsker knogleomsætningen må teoretisk formodes at øge risikoen for postoperativ hypokalkæmi. Til dato er der imidlertid kun publiceret få (retrospektive) studier, som har rapporteret modstridende resultater desangående (76-78). Da de fleste antiresorptive lægemidler deponeres i knoglevævet og udøver effekt længe efter ophør af behandlingen (79), vil evt. seponering umiddelbart forud for PTX næppe være af klinisk betydning. På baggrund heraf anbefales:
Allerede iværksat behandling af osteoporose med antiresorptive lægemidler fortsættes, men bør ikke iværksættes forud for PTX
(Evidensniveau IV)
9.2.2 Tilskud med kalcium forud for parathyreoidectomi
Et relativt højt kalciumindtag (800-1000 mg/dag) øger ikke plasma kalcium i forhold til et lavere dagligt indtag, hvorimod et lavt indtag kan føre til et øget PTH niveau og muligvis øge risikoen for nyresten (80;81). Som udgangspunkt anbefales:
Et dagligt indtag af kalk (fra kost og kosttilskud) på omkring 800-1000 mg.
(Evidensniveau IV)
Hos patienter med en forhøjet plasmakoncentration af 1,25(OH)2D er døgnurinudskillelsen af kalcium øget (81). Mhp. at mindske graden af hyperkalkuri, anbefales:
Hos patienter med plasma 1,25(OH)2D- over øvre referenceinterval tilstræbes et lavere indtag af kalcium (4-600 mg/dag).
(Evidensniveau IV)
Opmærksomheden henledes på at evt. kosttilskud med kalcium bør pauseres i relation til den biokemiske udredning
9.2.3 Tilskud med D-vitamin forud for parathyreoidectomi (Baggrundsartikel: 9.2.3.-VitD-PHPT-LRO-publiceret)
D-vitamindeficiens (plasma 25OHD < 25 nmol/l) og insufficiens (plasma 25OHD < 50 nmol/l) forekommer hyppigere hos patienter med PHPT end i baggrunds-befolkningen (27-29), medens plasma 1,25(OH)2D er højere (afsnit 5.1). Plasma PTH og kalcium koncentrationen såvel som koncentrationen af biokemiske knoglemarkører samt vægten af adenomer fjernet ved parathyreoidektomier er typisk højere hos patienter med PHPT og D-vitaminmangel end hos patienter med en sufficient D-vitaminstatus (27;82-86). Tillige er der rapporteret en invers association mellem den præoperative koncentration af 25OHD og risiko for postoperativt symptomgivende hypokalkæmi og SHPT (87;88). Hos enkelte patienter øger præoperativt tilskud med D-vitamin plasma og urin kalcium (89;90). Der foreligger ikke data fra RCT, som har undersøgt effekter af præoperativ substitutionsbehandling med D-vitamin (30;91). Det anbefales:
D-vitamininsufficiens bør undgås hos patienter med PHPT, hvorfor et dagligt tilskud på 10-20 μg D3-vitamin tilrådes ved P-25OHD < 50 nmol/l (71).
(Evidensniveau II)
9.2.4 Livsstilsforhold
Dehydrering og immobilisation bør undgås da dette kan føre til forværring af hyperkalkæmi og nyrefunktionspåvirkning. På baggrund heraf tilrådes foranstaltninger som anført i faktaboks 8.
Faktaboks 8. Præoperativ medicinsk håndtering af patienter med primær hyperparathyreoidisme
9.3 Kirurgisk parathyreoidektomi
Afhængig af den præoperative lokalisationsdiagnostik (afsnit 6.4) samt kendskab til ætiologi, planlægges et operative indgreb med den mindst mulige invasive procedure (92), som:
Bilateral halseksploration
Minimal invasiv parathyreoideakirurgi
Unilateral halseksploration
Et fokuseret indgreb
Patologiske kirtler fjernes skånsom in toto. Læderes kirtlen risikeres udsæd af patologisk væv.
9.3.1 Bilateral halseksploration
Ved proceduren foretages dobbeltsidig halseksploration med frilægning af alle fire parathyreoideakirtler gennem en hudincision på ca. 4-6 cm i midtlinjen. I udvalgte tilfælde med hyperplasi/flerglandelsygdom foretages subtotal PTX med fjernelse af 3-3½ glandel, herunder ved:
Hyperplasi (herunder ved tertiær hyperparathyreoidisme)
Familiære former for PHPT (afsnit 2.2 og 6.5.4)
Lithiuminduceret PHPT (afsnit 6.5.2) (93;94)
Metoden har hidtil været anset for guldstandard (95). I dag opereres dog kun en mindre andel med denne metode da adskillige studier har godtgjort at en mere målrettet (mindre invasiv) operativ teknik fører til en lige så høj succesrate (95-98).
9.3.2 Minimal invasiv parathyreoideakirurgi
Ved entydig præoperative sidelokalisation er succesraten ved et minimalt invasivt indgreb på niveau med succesraten ved bilateral halseksploration (98-103).
(Evidensniveau I)
Sammenlignet med bilateral halseksploration indebærer et minimalt invasivt indgreb tillige fordele som kortere operationsvarighed og indlæggelsestid, mindsket risiko for postoperativ hypokalkæmi, færre postoperative smerter og et forbedret kosmetisk resultat. Ved at mindske operationsområdet vil et evt. efterfølgende indgreb tillige lettere kunne gennemføres i områder hvor der ikke tidligere er opereret (95-99;103).
I en nylig dansk opgørelse som inkluderede 116 konsekutive patienter som fik foretaget PTX var den mediane operationstid for alle patienter 55 (spændvidde 15-180) min, mens den mediane operationstid for patienter som fik foretaget et fokuseret indgreb var 35 min. Patienterne var i gennemsnit indlagt i 1,05 døgn efter operationen (103).
9.3.2.1. Unilateral halseksploration
Ved proceduren visualiseres de 2 glandler på enten højre eller venstre side gennem en lille incision i enten midtlinjen eller på den side hvor et adenom mistænkes (103). Hvis der påvises adenomdannelse i blot én glandel fjernes denne. Findes et adenom ikke på den pågældende side udvides indgrebet til bilateral eksploration. Unilateral halseksploration foretrækkes:
Hvor parathyreoideaskintigrafi har givet mistanke om adenomdannelse på den ene side af halsen uden at dette er bekræftet ved ultralydsundersøgelse. Hvis der peroperativt ikke identificeres en patologisk kirtel, udvides indgrebet til en bilateral halseksploration.
Hvor UL-scanning og parathyreoideaskintigrafi har vist samstemmende sidelokalisation, men hvor der er tvivl om hvorvidt den syge glandel er beliggende superiort eller inferiort ved gld. thyreoidea – eller hvor 2 syge glandler på samme side mistænkes.
9.3.2.2. Fokuseret parathyroideakirurgi
Ved proceduren laves en lille incision ud for den glandel hvor der er påvist adenomdannelse. Proceduren foretrækkes:
Ved samstemmende resultater af UL-scanning og parathyreoideaskintigrafi tydende på en enkelt syg glandel beliggende enten superiort eller inferiort ved gld. thyreoidea.
9.3.3 Patologiske glandler i mediastinum
Patologiske glandler kan være lokaliseret anteriort/superiort i mediastinum. Patologiske kirtler i thymusrest kan sædvanligvis fjernes oppefra uden sternotomi. Til tider er det muligt at fjerne dybere liggende glandler ved en thorakoskopi, hvorved et mere invasivt indgreb i form af sternotomi kan undgås (104;105).
Faktaboks 9. Indikation for bilateral halseksploration

9.3.4 Specialiserede operationsteknikker
Det er forhåndenværende ikke dokumenteret, at det kirurgiske resultat bedres ved brug af specialiserede teknikker, herunder endoskopibaseret eller videoassisteret operationsteknik (106;107), radioguidet fokuseret operation (108;109) eller injektion af blåfarvet methylen. Methylen optages i adenomer og kan dermed facilitere en visuelle identifikation, men frarådes pga. mulige neurologiske bivirkninger (54;110-112).
9.3.5 Anæstesi ved parathyreoidectomi
Parathyreoideakirurgi udføres som udgangspunkt i general anæstesi (GA). Lokal anæstesi (LA) med let sedering af patienten og anlæggelse af infiltrationsanalgesi omkring incisionslinjen er dog muligt (113). Såvel et fokuseret indgreb som (sub-)total PTX kan foretages i LA (100;113-115). I en serie af udvalgte patienter, som fik foretaget minimal invasiv parathyroideakirurgi, blev der fundet et ligeværdigt behandlingsresultat ved LA og GA, men LA førte til færre postoperative gener i form smerter, kvalme og opkastninger (113;116). På baggrund af, at der ikke foreligger data fra randomiserede studier, anbefales:
Som standardprocedure anvendes GA ved PTX
LA kan overvejes hos patienter hvor GA anses for risikofyldt
(Evidensniveau IV)
9.3.6 Peroperative procedurer
Afhængig af karakteren af det kirurgiske indgreb kan der peroperativt anvendes frysemikroskopi, PTH-koncentrationsbestemmelse og identifikation af af nervus recurrens mhp. at bedre det operative resultat.
9.4 Reoperation for primær hyperparathyreoidisme
En PTX anses for at være vellykket, hvis patienten opnår normokalkæmi som vedvarer i minimum 6 måneder.
Fortsat PHPT efter intenderet kurativ PTX opdeles konceptionelt i (97):
Persisterende PHPT: Hyperparathyreoid hyperkalkæmi som konstateres umiddelbart efter operationen eller som recidiverer inden for 6 måneder postoperativt.
Recidiv af PHPH: Genkomst af PHPT efter mere end 6 måneder
9.4.1 Hyppighed af reoperation
Hos patienter som får foretaget PTX på et højtspecialiseret center, kan det forventes at 5-10 % af patienterne vil have behov for reoperation.
Ved langtidsopfølgning af patienter med sporadisk PHPT forekomemer recidiv hos op til 8 % efter 3-11 års opfølgning (97;117;118).
9.4.2 Tidspunkt for reoperation
Reoperation kan foretages i dagene umiddelbart efter det primære indgreb.
Hvis reoperation ikke fortages inden for 3-4 dage efter det primære indgreb, anbefales det at vente til 3-4 måneder efter det primære indgreb, idet den primære ardannelsen med fibrose herefter er mindre udtalt end i de første uger efter det primære indgreb (119).
(Evidensniveau III-IV)
9.4.3 Udredning forud for reoperation
Lokalisationsdiagnostik: som minimum foretages fornyet parathyreoideaskintigrafi med SPECT og ultralydsundersøgelse. Ved negative fund eller manglende overensstemmelse anbefales supplerende lokalisationsdiagnostik (afsnit 6.4.1) og i relation hertil vurderes om patienten kan have ektopisk beliggende patologiske glandler (112;120).
Genetisk testning: Hos patienter med vedvarende postoperativ hyperkalkæmi, trods en tilsyneladende vellykket operation anbefales genetisk testning for FHH uanset størrelsen af kalcium-kreatinin clearance ratio (afsnit 6.5.1). Ved negativt resultat suppleres om muligt med familiescreening. Tillige overvejes supplerende genetisk testning for familiære former for PHPT (afsnit 6.5.4).
9.4.4 Forventet resultat ved reoperation
Chancen for en vellykket operation en lidt mindre end ved førstegangskirurgi, men succesrate er oftest >90 % (75;112;114;119-121). Succesraten er i høj grad afhængig af hvorvidt det præoperativt er lykkes at identificere det patologiske parathyreoideavæv (122).
Reoperation er forbundet med en øget risiko for komplikationer (afsnit 10).
(Evidensniveau IV)
9.5 Kirurgisk behandling af særlige patientgrupper
9.5.1 Familiære former
Multiple endokrine neoplasier type 1 (MEN-1) og familiær isoleret hyperparathyreoidisme (FIHP): Ved sygdommene ses flerglandel hyperplasi, om end fordelingen kan være uensartet således at én af kirtlerne kan fremstå som større end de øvrige og (feljagtigt) blive anset for at være udtyk for adenomdannelse. Det anbefales
Subtotal PTX eller total PTX med autoimplantation af 50-60 mg kirtelvæv i en muskel på overarmen eller låret. Samtidigt foretages subtotal thymektomi mhp resektion af evt. surnummererede (ektopiske) parathyreoideaglandler (123). Trods velgennemført operation kan recidiv forventes hos op til 20 % af patienterne (124;125).
(Evidensniveau II)
Multiple endokrine neoplasier type 2 (MEN-2): PHPT er kun sjældent den primære manifestation ved MEN-2, men som oftes får patienterne udført total thyreoidectomi mhp. forebyggelse eller behandling af medullært thyreoideacarcinom. Da kun en mindre andel af patienterne (10-25%) udvikler PHPT er profylaktisk PTX ikke hensigtsmæssig (126-128).
Ved MEN-2 anbefales PTX kun ved tegn på manifest PHPT
9.5.2 Lithiumbehandling
Effekter af lithium på gll. parathyreoidea samt differentialdiagnostiske overvejelser forud for evt. operation er anført i afsnit 6.5.2.
Præoperativ lokalisationsdiagnostik
Lithiuminduceret hyperparathyreoidisme fører som oftes til hyperplasi af flere glandler, omend en glandel kan fremstå som dominerende ved dem præoperative billeddiagnostik (asymetrisk hypertrofi) (94).
Operativ procedure ved PTX hos patienter i lithiumbehandling
Hos patienter med lithiuminduceret hyperparathyreoidisme er der rapporteret en høj recidivrate hvis den primære operation udføres som et unilateralt/fokuseret indgreb, hvorfor der som udgangspunkt anbefales bilateral halseksploration med subtotal PTX (93;94;128;129).
(Evidensniveau IV)
9.5.3 Patienter med svær adipositas
I forhold til baggrundsbefolkningen har patienter med PHPT en højere vægt (32). Adipositas er associeret med et højere præoperativ PTH-niveau og vægten af fjernet parathyreoideavæv er gennemsnitligt højere (130;131).
Hos patienter med svær adipositas er der rapporteret en længere gennemsnitlig operationsvarighed, men succesraten (opnåelse af normokalcæmi), forekomsten af postoperative komplikationer og risikoen for recidivsygdom er den samme som hos patienter uden adipositas (130;131). Som udgangspunkt kan patienter med svær adipositas således tilbydes PTX i lighed med patienter uden svær overvægt.
9.5.4 Gravide
Forekomsten af PHPT hos gravide er ukendt. I verdenslitteraturen er der rapporteret mindre end 300 tilfælde. Imidlertid er sygdommen angiveligt underdiagnosticeret hos gravide. En stor andel er asymptomatiske (≈80 %) eller har blot uspecifikke symptomer som træthed og kvalme der let mistolkes som graviditets relaterede gener (132).
I flere studier er der rapporteret en øget risiko for intrauterin væksthæmning, føtale misdannelser og postnatal hypokalkæmi pga. en relativ suppression af fosterets parathyreoideaglandler (132;133).
Hos den gravide kvinde er der en øget risiko for nyresten, udvikling af hyperkalkæmisk krise og præeklamsi (134). Den til dato største opgørelse af gravide med PHPT er et observationelt studium som omfattede 77 gravide kvinder. I studiet blev det fundet, at kvinder som fik foretaget PTX (n=15) gennemførte den resterende del af graviditeten uden at der tilstødte komplikationer. I gruppen af kvinder som blev observeret uden PTX (n=62) aborterede 48 % svarende til at risikoen for abort var øget med en faktor 3,5 (135). Risikoen for abort var særligt øget i slutningen af 1.- samt i 2. trimester. Risikoen for abort korrelerede signifikant med plasma kalcium, med størst risiko hos kvinder med en (total) plasma kalciumkoncentration > 2,78 mmol/l Sv.t Ca+2 > 1,45 mmol/l). På baggrund heraf anbefales:
Hos gravide med PHPT anbefales PTX tidligt i 2. trimester.
Præoperativ lokalisationsdiagnostik foretages med ultralyd (parathyreoideaskintigrafi er kontraindiceret hos gravide).
Kalcium/kreatinin clearance ratio kan ikke bruges til diagnostik af FHH hos gravide. Det anbefales at alle får foretaget fremskyndet CaSR gen analyse med mindre ultralyd entydig tyder på adenom. FHH patienter opereres ikke, da subtotal PTX ikke påvirker plasma kalcium.
Umiddelbart postoperativt gives peroralt tilskud med kalcium i en dosis på 800-1200 mg/dag for at undgå postoperativ hypokalkæmi.
Det er uvist hvorledes kvinder som diagnosticeres med PHPT sent i graviditeten (3. trimester) bedst behandles (136). Adskillige kasuistiske meddelelser har dog rapporteret et vellykket resultat af PTX hos gravide i 3. trimester (132).
Hos gravide med (betydelig) symptomgivende hyperkalkæmi kan plasma kalcium mindskes med i.v.-infusion af calcitonin (krydser ikke placenta) og/eller peroralt fosfat tilskud i en dosis på 1.5-2.5 g/dag (mindsker den intestinal kalciumabsorption) (137).
Børn født af kvinder med ubehandlet PHPT observeres tæt i dagene efter fødslen pga. en øget risiko for hypoparathyroid hypokalkæmi (138).
(Evidensniveau IV)
9.5.5 Børn og unge
Det er estimeret at PHPT hos børn og unge forekommer med en incidens på 2-5 per 100.000 (139). Hos børn og unge forekommer hyperplasi/flerglandel sygdom hyppigere end hos voksne. Dette kan angiveligt tilskrives at PHPT hos børn og unge i større omfang end hos voksne er forårsaget af de familiære former for PHPT (afsnit 2.2) (140). I forhold til voksne er diagnostikken af sporadisk PHPT hos børn og unge ofte forsinket, da rutinemæssig biokemisk screening med bestemmelse af plasma kalcium kun anvendes i begrænset omfang hos børn. Børn diagnosticeres således typisk først, når de har udviklet betydelige symptomer (139-141). PTX kan foretages i alle aldre og med samme succesrate som hos voksne (142). Det er rapporteret at børn hurtigt opnår en normalisering af deres BMD efter PTX (143). Der foreligger ikke studier hvor børn/unge med PHPT er observeret over en længere tidsperiode uden PTX. På baggrund heraf anbefales:
Hos børn med PHPT tilstræbes umiddelbar operation mhp. kurativ PTX.
9.5.6 Kirurgisk behandling af patienter med høj alder
Hos ældre (>70-80 år) diagnosticeres PHPT ofte på et senere tidspunkt end hos yngre, idet symptomer typisk tilskrives aetas (144). I flere studier er det fundet, at andelen af patienter med asymptomatisk PHPT falder med stigende alder (144;145). Postoperativ opfølgning har dog vist at PTX hos ældre patienter kan resultere i en betydelig symptomlindring hvad angår klager som træthed, nyktturi, smerter fra bevægeapparatet, obstipation og depression (144;146;147).
Data fra USA tyder på, at ældre patienter med PHPT i mindre omfang end yngre patienter henvises til kirurgisk behandling (148). I de fleste studier er succesraten ved PTX hos ældre patienter på niveau med chancen for en vellykket operation hos yngre patienter (146;149). Risikoen for respiratoriske komplikationer ved operation i generel anæstesi er angiveligt øget hos ældre patienter (114;150).
Ældre patienter bør i lighed med yngre vurderes mhp. PTX, hvor det er vigtigt at være opmærksom på at der findes et stort overlap mellem symptomer som oftes tilskrives aetas og symptomer betinget af hyperkalkæmi.
Den øgede operationsrisiko hos ældre er i det væsentligste relateret til komplikationer ved generel anæstesi, hvorfor muligheden for at foretage PTX i lokal anæstesi bør overvejes.
(Evidensniveau II)
Referencer
(27) Moosgaard B, Vestergaard P, Heickendorff L, Melsen F, Christiansen P, Mosekilde L. Vitamin D status, seasonal variations, parathyroid adenoma weight and bone mineral density in primary hyperparathyroidism. Clinical Endocrinology. 2005;63:506-13.
(28) Silverberg SJ. Vitamin D deficiency and primary hyperparathyroidism. J Bone Miner Res. 2007;22 Suppl 2:V100-V104.
(29) Farahnak P, Lärfars G, Sten-Linder M, Nilsson IL. Mild Primary Hyperparathyroidism: Vitamin D Deficiency and Cardiovascular Risk Markers. Journal of Clinical Endocrinology & Metabolism. 2011;96:2112-18.
(30) Rolighed L, Bollerslev J, Mosekilde L. Vitamin D treatment in primary hyperparathyroidism. Curr Drug Saf. 2011;6:100-107.
(32) Bolland MJ, Grey AB, Gamble GD, Reid IR. Association between Primary Hyperparathyroidism and Increased Body Weight: A Meta-Analysis. Journal of Clinical Endocrinology Metabolism. 2005;90:1525-30.
(54) Harrison B, Triponez F. Intraoperative adjuncts in surgery for primary hyperparathyroidism. Langenbeck’s Archives of Surgery. 2009;394:799-809.
(71) Bilezikian JP, Khan AA, Potts JT, Jr., on behalf of the Third International Workshop on the Management of Asymptomatic Primary Hyperthyroidism. Guidelines for the Management of Asymptomatic Primary Hyperparathyroidism: Summary Statement from the Third International Workshop. Journal of Clinical Endocrinology Metabolism. 2009;94:335-39.
(72) Udelsman R, Pasieka JL, Sturgeon C, Young JEM, Clark OH. Surgery for Asymptomatic Primary Hyperparathyroidism: Proceedings of the Third International Workshop. Journal of Clinical Endocrinology Metabolism. 2009;94:366-72.
(73) Silverberg SJ, Lewiecki EM, Mosekilde L, Peacock M, Rubin MR. Presentation of Asymptomatic Primary Hyperparathyroidism: Proceedings of the Third International Workshop. Journal of Clinical Endocrinology Metabolism. 2009;94:351-65.
(74) Ruda JM, Hollenbeak CS, Stack BC. A systematic review of the diagnosis and treatment of primary hyperparathyroidism from 1995 to 2003. Otolaryngology — Head and Neck Surgery. 2005;132:359-72.
(75) Bergenfelz A, Jansson S, Mårtensson H, Reihnér E, Wallin G, Kristoffersson A et al. Scandinavian quality register for thyroid and parathyroid surgery: audit of surgery for primary hyperparathyroidism. Langenbeck’s Archives of Surgery. 2007;392:445-51.
(76) Corsello SM, Paragliola RM, Locantore P, Ingraudo F, Ricciato MP, Rota CA et al. Post-surgery severe hypocalcemia in primary hyperparathyroidism preoperatively treated with zoledronic acid. Hormones (Athens ). 2010;9:338-42.
(77) Lee IT, Sheu WH-H, Tu ST, Kuo SW, Pei D. Bisphosphonate pretreatment attenuates hungry bone syndrome postoperatively in subjects with primary hyperparathyroidism. Journal of Bone and Mineral Metabolism. 2006;24:255-58.
(78) Davenport A, Stearns MP. Administration of pamidronate helps prevent immediate postparathyroidectomy hungry bone syndrome. Nephrology. 2007;12:386-90.
(79) Fleisch HA. Bisphosphonates: preclinical aspects and use in osteoporosis. Ann Med. 1997;29:55-62.
(80) Borghi L, Schianchi T, Meschi T, Guerra A, Allegri F, Maggiore U et al. Comparison of Two Diets for the Prevention of Recurrent Stones in Idiopathic Hypercalciuria. N Engl J Med. 2002;346:77-84.
(81) Locker FG, Silverberg SJ, Bilezikian JP. Optimal Dietary Calcium Intake in Primary Hyperparathyroidism. The American Journal of Medicine. 1997;102:543-50.
(82) Silverberg SJ, Shane E, Dempster DW, Bilezikian JP. The effects of vitamin D insufficiency in patients with primary hyperparathyroidism. Am J Med. 1999;107:561-67.
(83) Rao DS, Honasoge M, Divine GW, Phillips ER, Lee MW, Ansari MR et al. Effect of vitamin D nutrition on parathyroid adenoma weight: pathogenetic and clinical implications. J Clin Endocrinol Metab. 2000;85:1054-58.
(84) Ozbey N, Erbil Y, Ademoglu E, Ozarmagan S, Barbaros U, Bozbora A. Correlations between vitamin D status and biochemical/clinical and pathological parameters in primary hyperparathyroidism. World J Surg. 2006;30:321-26.
(85) Beyer TD, Chen EL, Nilubol N, Prinz RA, Solorzano CC. Short-Term Outcomes of Parathyroidectomy in Patients With or Without 25-Hydroxy Vitamin D Insufficiency. Journal of Surgical Research. 2007;143:145-50.
(86) Stein EM, Dempster DW, Udesky J, Zhou H, Bilezikian JP, Shane E et al. Vitamin D deficiency influences histomorphometric features of bone in primary hyperparathyroidism. Bone. 2011;48:557-61.
(87) Stewart ZA, Blackford A, Somervell H, Friedman K, Garrett-Mayer E, Dackiw AP et al. 25-hydroxyvitamin D deficiency is a risk factor for symptoms of postoperative hypocalcemia and secondary hyperparathyroidism after minimally invasive parathyroidectomy. Surgery. 2005;138:1018-25.
(88) Untch BR, Barfield ME, Dar M, Dixit D, Leight J, Olson J. Impact of 25-Hydroxyvitamin D Deficiency on Perioperative Parathyroid Hormone Kinetics and Results in Patients with Primary Hyperparathyroidism. Surgery. 2007;142:1022-26.
(89) Grubbs EG, Rafeeq S, Jimenez C, Feng L, Lee JE, Evans DB et al. Preoperative vitamin D replacement therapy in primary hyperparathyroidism: safe and beneficial? Surgery. 2008;144:852-58.
(90) Isidro M, Ruano Bn. Biochemical effects of calcifediol supplementation in mild, asymptomatic, hyperparathyroidism with concomitant vitamin D deficiency. Endocrine. 2009.
(91) Mikhail N. Clinical significance of vitamin D deficiency in primary hyperparathyroidism, and safety of vitamin D therapy. South Med J. 2011;104:29-33.
(92) Lew JI, Solorzano CC. Surgical Management of Primary Hyperparathyroidism: State of the Art. Surg Clin North Am. 2009;89:1205-25.
(93) Hundley JC, Woodrum DT, Saunders BD, Doherty GM, Gauger PG. Revisiting lithium-associated hyperparathyroidism in the era of intraoperative parathyroid hormone monitoring. Surgery. 2005;138:1027-32.
(94) Skandarajah A, Palazzo F, Henry JF. Lithium-Associated Hyperparathyroidism: Surgical Strategies in the Era of Minimally Invasive Parathyroidectomy. World Journal of Surgery. 2011;35:2432-39.
(95) Christiansen P, Mollerup CL. Ny teknik ved behandling af primær hyperparatyroidisme. Ugeskr Laeger. 2005;167:918-24.
(96) Udelsman R. Six hundred fifty-six consecutive explorations for primary hyperparathyroidism. Ann Surg. 2002;235:665-70.
(97) Irvin GL, III, Carneiro DM, Solorzano CC. Progress in the operative management of sporadic primary hyperparathyroidism over 34 years. Ann Surg. 2004;239:704-8.
(98) Beyer TD, Solorzano CC, Starr F, Nilubol N, Prinz RA. Parathyroidectomy outcomes according to operative approach. The American Journal of Surgery. 2007;193:368-73.
(99) Bergenfelz A, Lindblom P, Tibblin S, Westerdahl J. Unilateral versus bilateral neck exploration for primary hyperparathyroidism: a prospective randomized controlled trial. Ann Surg. 2002;236:543-51.
(100) Bergenfelz A, Kanngiesser V, Zielke A, Nies C, Rothmund M. Conventional bilateral cervical exploration versus open minimally invasive parathyroidectomy under local anaesthesia for primary hyperparathyroidism. Br J Surg. 2005;92:190-197.
(101) Russell CFJ, Dolan SJ, Laird JD. Randomized clinical trial comparing scan-directed unilateral versus bilateral cervical exploration for primary hyperparathyroidism due to solitary adenoma. Br J Surg. 2006;93:418-21.
(102) Westerdahl J, Bergenfelz A. Unilateral versus bilateral neck exploration for primary hyperparathyroidism: five-year follow-up of a randomized controlled trial. Ann Surg. 2007;246:976-80.
(103) Trolle W, Moller H, Bennedbaek FN, Nygaard B, Sorensen CH. Minimalt invasiv operation for hyperparathyroidisme. Ugeskr Laeger. 2010;172:33-38.
(104) Kumar A, Kumar S, Aggarwal S, Kumar R, Tandon N. Thoracoscopy: the preferred method for excision of mediastinal parathyroids. Surg Laparosc Endosc Percutan Tech. 2002;12:295-300.
(105) Harrison B. What steps should be considered in the patient who has had a negative cervical exploration for primary hyperparathyroidism? Clinical Endocrinology. 2009;71:624-27.
(106) Hessman O, Westerdahl J, Al Suliman N, Christiansen P, Hellman P, Bergenfelz A. Randomized clinical trial comparing open with video-assisted minimally invasive parathyroid surgery for primary hyperparathyroidism. Br J Surg. 2010;97:177-84.
(107) Gracie D, Hussain SSM. Use of minimally invasive parathyroidectomy techniques in sporadic primary hyperparathyroidism: systematic review. The Journal of Laryngology & Otology. 2011;1:1-7.
(108) Rubello D, Mariani G, Pelizzo MR. Minimally invasive radio-guided parathyroidectomy on a group of 452 primary hyperparathyroid patients: refinement of preoperative imaging and intraoperative procedure. Nuklearmedizin. 2007;46:85-92.
(109) Rubello D, Giannini S, De Carlo E, Mariani G, Muzzio PC, Rampin L et al. Minimally invasive (99m)Tc-sestamibi radioguided surgery of parathyroid adenomas. Panminerva Med. 2005;47:99-107.
(110) Han N, Bumpous JM, Goldstein RE, Fleming MM, Flynn MB. Intra-Operative Parathyroid Identification Using Methylene Blue in Parathyroid Surgery. The American surgeon. 2007;73:820-823.
(111) Licker M, Diaper J, Robert J, Ellenberger C. Effects of methylene blue on propofol requirement during anaesthesia induction and surgery. Anaesthesia. 2008;63:352-57.
(112) Bergenfelz A, Hellman P, Harrison B, Sitges-Serra A, Dralle H. Positional statement of the European Society of Endocrine Surgeons (ESES) on modern techniques in pHPT surgery. Langenbeck’s Archives of Surgery. 2009;394:761-64.
(113) Carling T, Donovan P, Rinder C, Udelsman R. Minimally Invasive Parathyroidectomy Using Cervical Block: Reasons for Conversion to General Anesthesia. Arch Surg. 2006;141:401-4.
(114) Allendorf J, DiGorgi M, Spanknebel K, Inabnet W, Chabot J, LoGerfo P. 1112 Consecutive Bilateral Neck Explorations for Primary Hyperparathyroidism. World Journal of Surgery. 2007;31:2075-80.
(115) Cheong YT, Taib NA, Normayah K, Hisham AN. Total Parathyroidectomy Under Local Anaesthesia for Renal Hyperparathyroidism. Asian Journal of Surgery. 2009;32:51-54.
(116) Chau JK, Hoy M, Tsui B, Harris JR. Minimally invasive parathyroidectomy under local anesthesia: patient satisfaction and overall outcome. J Otolaryngol Head Neck Surg. 2010;39:361-69.
(117) Clerici T, Kull C, Sege D, Rittmann WW. [Incidence of recurrence in long-term follow-up of 100 patients after surgery for primary hyperparathyroidism]. Helv Chir Acta. 1992;58:767-70.
(118) Amstrup AK, Rejnmark L, Vestergaard P, Sikjaer T, Rolighed L, Heickendorff L et al. Vitamin D status, physical performance and body mass in patients surgically cured for primary hyperparathyroidism compared with healthy controls – a cross-sectional study. Clin Endocrinol (Oxf). 2011;74:130-136.
(119) Sarfati E, Billotey C, Halimi B, Fritsch S, Cattan P, Dubost C. Early localization and reoperation for persistent primary hyperparathyroidism. Br J Surg. 1997;84:98-100.
(120) Hessman O, Stålberg P, Sundin A, Garske U, Rudberg C, Eriksson LG et al. High Success Rate of Parathyroid Reoperation may be Achieved with Improved Localization Diagnosis. World Journal of Surgery. 2008;32:774-81.
(121) Henry JF. Reoperation for primary hyperparathyroidism: tips and tricks. Langenbecks Arch Surg. 2010;395:103-9.
(122) Wells SA, Jr., Debenedetti MK, Doherty GM. Recurrent or persistent hyperparathyroidism. J Bone Miner Res. 2002;17 Suppl 2:N158-N162.
(123) Hubbard J, Sebag Fdr, Maweja S, Henry JF. Primary hyperparathyroidism in MEN 1 – how radical should surgery be? Langenbeck’s Archives of Surgery. 2002;386:553-57.
(124) Goudet P, Cougard P, Verges B, Murat A, Carnaille B, Calender A et al. Hyperparathyroidism in multiple endocrine neoplasia type I: surgical trends and results of a 256-patient series from Groupe D’etude des Neoplasies Endocriniennes Multiples Study Group. World J Surg. 2001;25:886-90.
(125) Hellman P, Skogseid B, Oberg K, Juhlin C, Akerstrom G, Rastad J. Primary and reoperative parathyroid operations in hyperparathyroidism of multiple endocrine neoplasia type 1. Surgery. 1998;124:993-99.
(126) Frank-Raue K, Raue F. Multiple endocrine neoplasia type 2 (MEN 2). European Journal of Cancer. 2009;45, Supplement 1:267-73.
(127) Tonelli F, Marcucci T, Giudici F, Falchetti A, Brandi ML. Surgical Approach in Hereditary Hyperparathyroidism. Endocrine Journal. 2009;56:827-41.
(128) Åkerstrøm G. Symposium on Evidence-Based Endocrine Surgery (3: Hyperparathyroidism). World Journal of Surgery. 2009;33:2219-23.
(129) Saunders B, Saunders E, Gauger P. Lithium Therapy and Hyperparathyroidism: An Evidence-Based Assessment. World Journal of Surgery. 2009;33:2314-23.
(130) Pitt SC, Panneerselvan R, Sippel RS, Chen H. Influence of morbid obesity on parathyroidectomy outcomes in primary hyperparathyroidism. The American Journal of Surgery. 2010;199:410-415.
(131) Norman J, Aronson K. Outpatient parathyroid surgery and the differences seen in the morbidly obese. Otolaryngology — Head and Neck Surgery. 2007;136:282-86.
(132) Schnatz PF, Curry SL. Primary hyperparathyroidism in pregnancy: evidence-based management. Obstet Gynecol Surv. 2002;57:365-76.
(133) Kohlmeier L, Marcus R. Calcium disorders of pregnancy. Endocrinol Metab Clin North Am. 1995;24:15-39.
(134) Hultin H, Hellman P, Lundgren E, Olovsson M, Ekbom A, Rastad J et al. Association of Parathyroid Adenoma and Pregnancy with Preeclampsia. Journal of Clinical Endocrinology & Metabolism. 2009;94:3394-99.
(135) Norman J, Politz D, Politz L. Hyperparathyroidism during pregnancy and the effect of rising calcium on pregnancy loss: a call for earlier intervention. Clin Endocrinol (Oxf). 2009;71:104-9.
(136) Ficinski ML, Mestman JH. Primary hyperparathyroidism during pregnancy. Endocr Pract. 1996;2:362-67.
(137) Montoro MN, Collea JV, Mestman JH. Management of hyperparathyroidism in pregnancy with oral phosphate therapy. Obstet Gynecol. 1980;55:431-34.
(138) Nilsson IL, Adner N, Reihnér E, Palme-Kilander C, Edstrom G, Degerblad M. Primary Hyperparathyroidism in Pregnancy: A Diagnostic and Therapeutic Challenge. Journal of Women’s Health. 2010;19:1117-21.
(139) Kollars J, Zarroug AE, van Heerden J, Lteif A, Stavlo P, Suarez L et al. Primary Hyperparathyroidism in Pediatric Patients. Pediatrics. 2005;115:974-80.
(140) Loh KC, Duh QY, Shoback D, Gee L, Siperstein A, Clark OH. Clinical profile of primary hyperparathyroidism in adolescents and young adults. Clinical Endocrinology. 1998;48:435-43.
(141) Rapaport D, Ziv Y, Rubin M, Huminer D, Dintsman M. Primary hyperparathyroidism in children. J Pediatr Surg. 1986;21:395-97.
(142) Cupisti K, Raffel A, Dotzenrath C, Krausch M, R+Âher HD, Schulte KM. Primary Hyperparathyroidism in the Young Age Group: Particularities of Diagnostic and Therapeutic Schemes. World Journal of Surgery. 2004;28:1153-56.
(143) Vanstone MB, Udelsman RD, Cheng DW, Carpenter TO. Rapid Correction of Bone Mass after Parathyroidectomy in an Adolescent with Primary Hyperparathyroidism. Journal of Clinical Endocrinology & Metabolism. 2011;96:E347-E350.
(144) Kebebew E, Duh QY, Clark OH. Parathyroidectomy for Primary Hyperparathyroidism in Octogenarians and Nonagenarians: A Plea for Early Surgical Referral. Arch Surg. 2003;138:867-71.
(145) Chen H, Parkerson S, Udelsman R. Parathyroidectomy in the Elderly: Do the Benefits Outweigh the Risks? World Journal of Surgery. 1998;22:531-36.
(146) Chigot JP, Menegaux F, Achrafi H. Should primary hyperparathyroidism be treated surgically in elderly patients older than 75 years? Surgery. 1995;117:397-401.
(147) Udén P, Chan A, Duh QY, Siperstein A, Clark OH. Primary hyperparathyroidism in younger and older patients: Symptoms and outcome of surgery. World Journal of Surgery. 1992;16:791-97.
(148) Wu B, Haigh PI, Hwang R, Ituarte PHG, Liu ILA, Hahn TJ et al. Underutilization of Parathyroidectomy in Elderly Patients with Primary Hyperparathyroidism. Journal of Clinical Endocrinology Metabolism. 2010;95:4324-30.
(149) Politz D, Norman J. Hyperparathyroidism in Patients Over 80: Clinical Characteristics and Their Ability to Undergo Outpatient Parathyroidectomy. Thyroid. 2007;17:333-39.
(150) Thomas DC, Roman SA, Sosa JA. Parathyroidectomy in the Elderly: Analysis of 7313 Patients. Journal of Surgical Research. 2011;170:240-246.

 Faktaboks 2. Biokemiske profik ved sygdom i gll. parathyreoidea
Faktaboks 2. Biokemiske profik ved sygdom i gll. parathyreoidea Referencer
Referencer Baggrundsartkel mangles grundet rettelser og copy-right
Baggrundsartkel mangles grundet rettelser og copy-right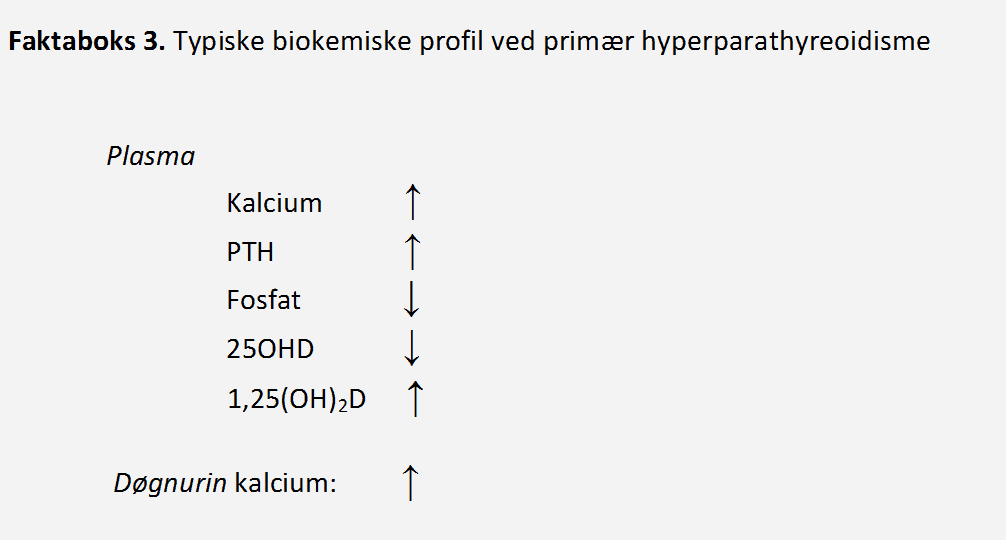 Plasma PTH: PHPT må mistænkes hos en patient med hyperkalkæmi og en plasma PTH koncentration som er forhøjet eller i øverste 1/3 af referenceområdet (typisk > 5 pmol/l). Dette fordi normalområdet for PTH er dårligt defineret idet der ved fastlæggelse af referenceintervallet ikke altid er taget hensyn til, at der i befolkningen er en høj prævalens af D-vitaminmangel med sekundær hyperparathyreoidisme (23-25). I diagnostisk henseende er det således ikke påkrævet at PTH koncentrationen er højere end øvre referenceinterval. Ved bestemmelse af plasma PTH anses 2. og 3. generations PTH assays for at være ligeværdige (23).
Plasma PTH: PHPT må mistænkes hos en patient med hyperkalkæmi og en plasma PTH koncentration som er forhøjet eller i øverste 1/3 af referenceområdet (typisk > 5 pmol/l). Dette fordi normalområdet for PTH er dårligt defineret idet der ved fastlæggelse af referenceintervallet ikke altid er taget hensyn til, at der i befolkningen er en høj prævalens af D-vitaminmangel med sekundær hyperparathyreoidisme (23-25). I diagnostisk henseende er det således ikke påkrævet at PTH koncentrationen er højere end øvre referenceinterval. Ved bestemmelse af plasma PTH anses 2. og 3. generations PTH assays for at være ligeværdige (23). Som anført i Tabel 3 er PHPT associeret med en øget risiko for en række følgetilstande og sygdomme.
Som anført i Tabel 3 er PHPT associeret med en øget risiko for en række følgetilstande og sygdomme.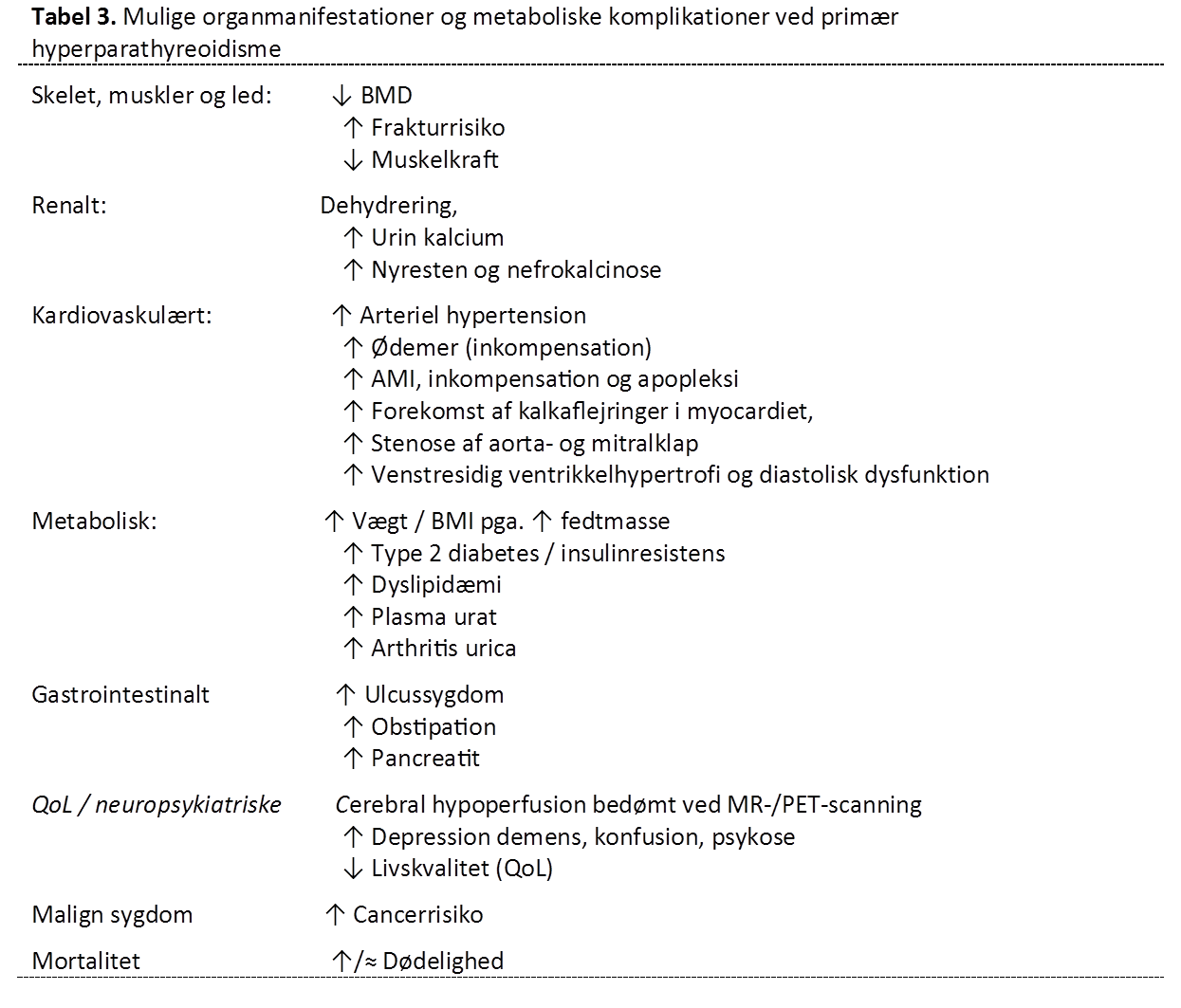 Referencer
Referencer



 6.5.1 Familiær hypokalkurisk hyperkalkæmi (FHH)
6.5.1 Familiær hypokalkurisk hyperkalkæmi (FHH)



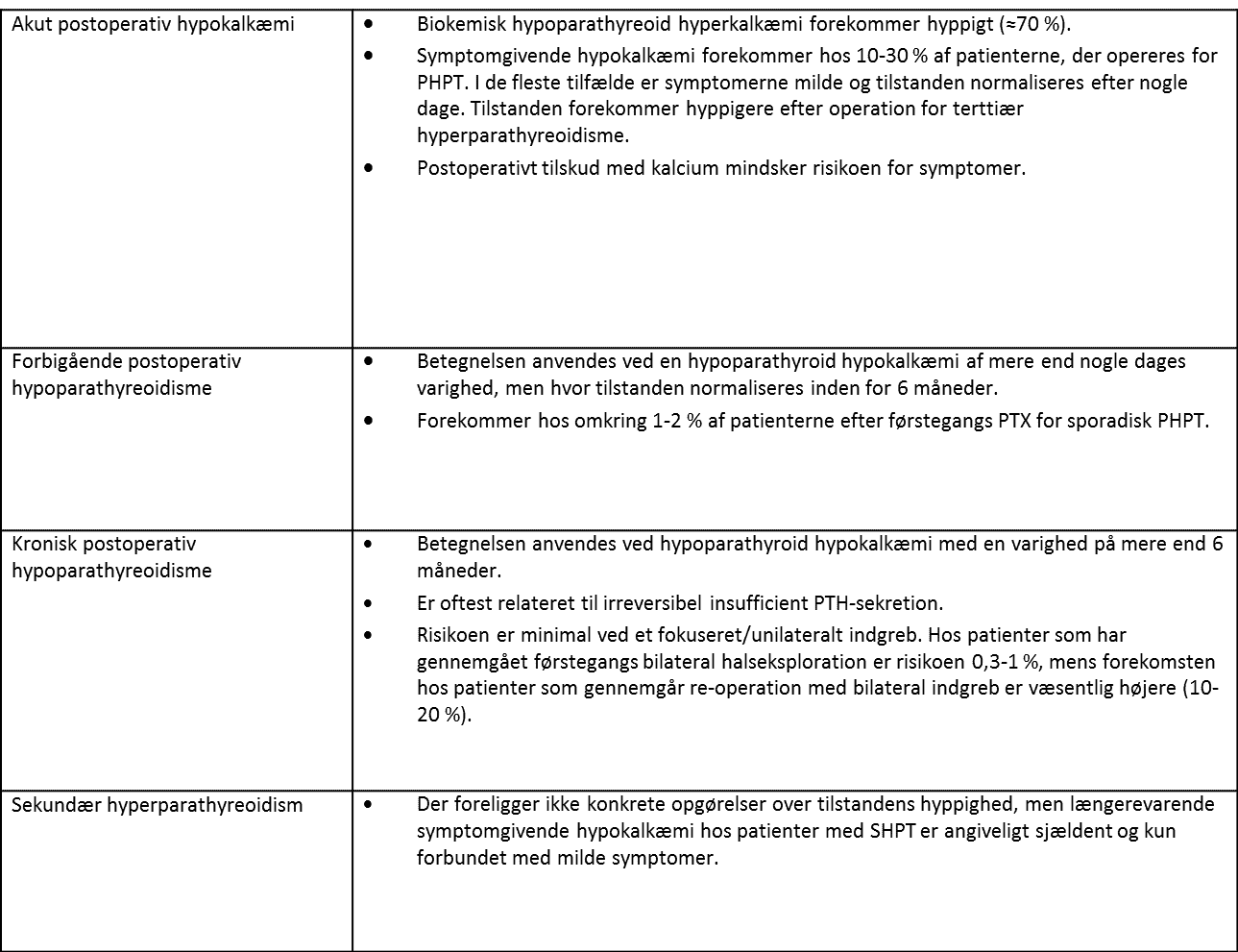 10.6 Forbigående hyperthyreoidisme
10.6 Forbigående hyperthyreoidisme

 11.4 Justering af anden medicinsk behandling.
11.4 Justering af anden medicinsk behandling. Referencer
Referencer Referencer
Referencer 14.1 Antiresorptiv behandling ved medicinsk observation
14.1 Antiresorptiv behandling ved medicinsk observation